CIRCUNSTANCIAS ACTUALES
En poco más de dos meses, la Bordetella pertussis, nombre científico de la bacteria que causa la tosferina, ha provocado la muerte de 4 bebés: dos en Andalucía, un tercero en Castilla-León y el más reciente en Madrid (3/12/2015). En siete CCAA (Asturias, Canarias, Cataluña, Comunidad Valenciana, Extremadura, Navarra y País Vasco) ya está implantado un programa de vacunación con dTpa (Boostrix® y Triaxis®) que además de ofrecer protección contra el tétanos (T) y la difteria(d), incluye la vacuna acelular contra la tosferina(pa), a mujeres embarazadas entre 27 y 36 semanas de embarazo, precisamente para evitar casos de tosferina en bebés menores de 2 meses que no han iniciado aún, lógicamente, el calendario vacunal y son susceptibles a la enfermedad.
Esta vacunación durante el embarazo no sustituye a la sistemática vacunación del bebé posterior al nacimiento. Se recomienda la vacunación en todos los embarazos, aunque haya pasado poco tiempo entre dos consecutivos y no se tendrá en cuenta los antecedentes vacunales frente a tétanos, difteria y tosferina. Cataluña fue la comunidad autónoma pionera en su implantación en enero del 2014 y ha alcanzado en la actualidad una cobertura del 66 % en embarazadas (datos del Institut Català de la Salut, ver enlace). En el Reino Unido comenzaron con este tipo de estrategia el 15 de octubre del 2012, con una campaña dirigida a la población y a los profesionales sanitarios. Es probable, además, que en el contexto de escasez mundial de vacunas dTpa, se retrase el recuerdo que era habitual sobre los 4-6 años de edad, sin que esto tenga repercusiones importantes, para precisamente priorizar su dispensación al colectivo de mujeres embarazadas, como ya se está haciendo en algunas CCAA.
DEFINICIÓN-CONCEPTO Y EPIDEMIOLOGÍA
La tosferina es una enfermedad muy contagiosa (alcanza al 80-90% de individuos susceptibles) que afecta al tracto respiratorio y se caracteriza por accesos de tos muy seca en paroxismos. Afecta a cualquier grupo de edad y sigue siendo una causa significativa de mortalidad y morbilidad en menores de 2 años. En los años anteriores a la vacunación el número de casos nuevos de enfermedad típica al año era similar al tamaño de una cohorte de nacidos en un año y casi todos los niños se habían infectado entre el año y los cinco años de edad.
Una de las estrategias para evitar su incidencia es la vacunación sistemática de los bebés (2 ,4 y 6 meses) y proporcionar tres dosis de recuerdo; la primera a los 18 meses, la segunda a los niños con 4-6 años y otra más sobre los 14 (esta última no se da en todas las CCAA por ofrecer la Td (tétanos y difteria), sin el componente de tosferina (pa). No obstante, la AEP propone para el cercano 2016, unas nuevas pautas que podrá ver aquí. Además, la vacunación en el embarazo transfiere al feto los anticuerpos necesarios para que durante los primeros 60 días, antes de recibir su primera dosis el bebé, disponga ya de las defensas necesarias para no infectarse y sufrir la enfermedad que es potencialmente mortal como ha sucedido en estos desgraciados casos. La Agencia de Salud Pública de Cataluña comenzó en enero del 2014 este programa mientras que en EEUU y en el Reino Unido, entre otros países, se había iniciado sobre los años 2011-2012.
La incidencia mundial anual de la tos ferina se estima en 48,5 millones de casos, con una tasa de mortalidad de casi 295.000 muertes por año. La tasa de letalidad entre los niños en los países de bajos ingresos puede ser de hasta un 4%. En Inglaterra, el porcentaje de personas vacunadas contra la tos ferina en los últimos 4 décadas se ha reducido a menos del 30%. Este descenso se ha traducido en miles de casos recientemente reportados de la enfermedad, con la tasa de incidencia próxima a la de la era prevacunal. Han ocurrido brotes epidémicos similares recientemente en Suecia, Canadá y Alemania.
Se cree que en África han ocurrido cerca de 300.000 muertes por tosferina durante la última década. Entre los años 2001-2003, de los pacientes con tos ferina en Estados Unidos, el 23% eran menores de 1 año, el 12% tenía una edad entre 1 y 4 años, el 9% tenían entre 5 y 9 años, el 33% tenía una edad de 10-19 años, y el 23% eran mayores de 20 años. Debido a la falta de transferencia de la inmunidad materna, el 10-15% de todos los casos de tosferina ocurren en bebés menores de 6 meses; más del 90% de todas las muertes ocurren en este mismo grupo de edad. Sin embargo, la mayoría de los casos se encuentran en las personas de 10 años o más, lo que ha llevado a un aumento de las recomendaciones de dosis vacunales de refuerzo para esas edades.
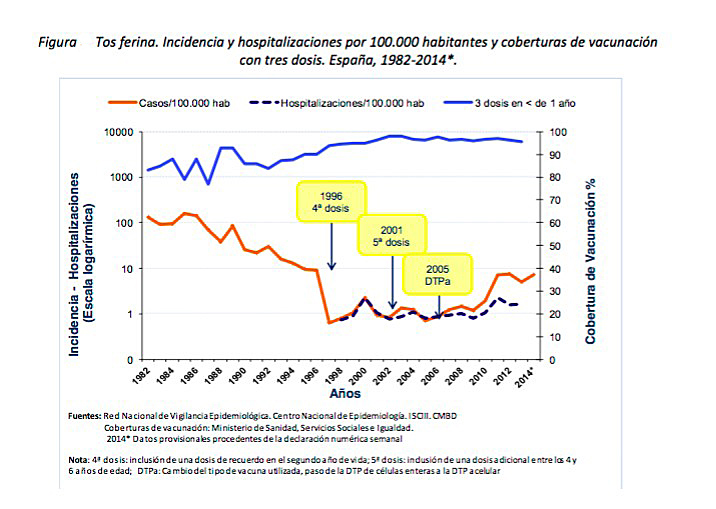
En España ha habido un descenso importante de la incidencia de la enfermedad a medida que las coberturas vacunales se han ido incrementando hasta 2008, año a partir del cual la incidencia ha ido aumentando progresivamente. En el año 2012, 2013 y 2014 se declararon 3.430, 2.342 y 3.262 casos respectivamente, con unas incidencias por 100.000 habitantes de 7,43, 5,03 y 7,18. A fecha de 22/11/2015 ya se han declarado en España 7.224 casos lo que muestra esa franca tendencia al aumento. Debemos tener en cuenta que esas incidencias podrían ser mayores debido al infradiagnóstico de la enfermedad, especialmente en adolescentes y adultos, en los que el bajo grado de sospecha (pueden pasar como catarros con tos molesta durante uno o dos meses) y las dificultades en el diagnóstico podrían hacer que la carga real de la enfermedad fuera bastante mayor de la que se está registrando.
La vacuna actual solo confiere protección para unos 5-6 años pues a los 4 años de la vacunación (son necesarias un mínimo de dos dosis para ser eficaz) la protección es del 84 % y los 7 años baja al 46 %. El principal origen de la infección en niños son los familiares que conviven con ellos, sobre todo los hermanos mayores -si los hay- y los mismos padres. No parecen existir portadores sanos. En esta gráfica podemos constatar este aumento global de la incidencia de tosferina desde el 2005- 2006 :
La letalidad, es decir, el número de muertes por la enfermedad podemos verla reflejada en esta tabla:

Todos los pediatras en estos últimos años han visto casos de bebés con tosferina que han necesitado ingreso y han comprobado el sufrimiento y el miedo que provoca esta enfermedad ya que los accesos de tos y las apneas -entre otro tipo de complicaciones- son verdaderamente impactantes. La tosferina es mortal en alrededor del 1,6 por ciento de los niños menores de un año hospitalizados.
APUNTES HISTÓRICOS
Aunque Guillaume de Baillou comenzó a describir la clínica de la tosferina en el año 1578 con el nombre de tussis quinta (por los accesos de salvas o series de tos en número aproximado de cinco) la historia moderna de este bicho con tan mala leche comienza en Bélgica en el año 1900 cuando el belga Jules Bordet (1870-1961) y el francés Octave Gengou (1875-1957) describen en sus estudios perfectamente esta bacteria a partir del esputo de un niño enfermo de 5 meses de edad; aunque similar a otra bacteria, que ya tenían fichada los microbiólogos de la época, denominada Haemophillus influenzae, la separan como género propio e independiente, y consiguen aislarla 6 años más tarde (no era fácil) en un cultivo compuesto por glicerol, patata, agar, solución salina y un volumen igual de sangre desfibrinada humana o de conejo (posteriormente se solía preferir sangre de carnero). La sangre adicionaba factores de crecimiento esenciales, el almidón de la patata absorbería los ácidos grasos que puedan estar presentes en las secreciones nasales o en el algodón de la torunda recogida, además de proporcionar nitrógeno y vitaminas, y el glicerol representaba una fuente de carbono. Por cierto, el “voluntario” que proporcionó el material fue nada más y nada menos que Paul, hijo de Bordet, en su primer día de tosferina (el ser hijo de investigador no le eximió de ser atacado por la bacteria de marras al igual que los hijos de pediatras también tienen mocos y alguna bronquitis como es normal). Hasta entonces, los investigadores pensaban que el responsable de esta enfermedad era un hongo (Letzerich 1870), pero Burger ya lo describió en 1883 como un bacilo pequeño y elipsoidal.
En 1887 Afanassjew, Czapleweski y Hensel, también lo identificaron pero no pudieron aislarlo; es decir, separarlo de su medio original —moco y secreciones nasofaríngeas— y hacerle crecer, reproducirse y observar detenidamente su estructura y su ciclo vital para así poder idear estrategias y métodos para evitar que nos infecte o, en su defecto, diseñar una vacuna para no sufrir la enfermedad estimulando el sistema inmunológico.
El Sr. Jules Jean Baptiste Vincent Bordet (1870-1961) se licenció en Física y en Medicina, dedicándose (como ha podido comprobar, con bastante denuedo y entusiasmo) a la Inmunología y a la Microbiología, de tal manera que llegó a conseguir el premio Nobel de Fisiología y Medicina en el año 1919. Además de identificar y aislar a la bacteria productora de la tosferina que recibiría finalmente su nombre (Bordet-ella), consiguió demostrar la capacidad bactericida del suero de la sangre de los mamíferos, y contribuyó a sentar las bases de la inmunología (junto con gigantes como Jenner, Koch y Pasteur) describiendo un componente sérico relacionado con la respuesta inmunitaria al que bautiza como “alexina”, caracterizado frente al anticuerpo por su termolabilidad e inespecificidad (más tarde recibió el nombre de complemento, propuesto por Ehrlich), además de desarrollar -sin mucho éxito- la primera vacuna contra esta enfermedad. El apellido de esta señorita bacteria siguió siendo el original propuesto ya en 1679 por el médico inglés Thomas Sydenham, pertussis (por provocar mucha tos, claro).
se licenció en Física y en Medicina, dedicándose (como ha podido comprobar, con bastante denuedo y entusiasmo) a la Inmunología y a la Microbiología, de tal manera que llegó a conseguir el premio Nobel de Fisiología y Medicina en el año 1919. Además de identificar y aislar a la bacteria productora de la tosferina que recibiría finalmente su nombre (Bordet-ella), consiguió demostrar la capacidad bactericida del suero de la sangre de los mamíferos, y contribuyó a sentar las bases de la inmunología (junto con gigantes como Jenner, Koch y Pasteur) describiendo un componente sérico relacionado con la respuesta inmunitaria al que bautiza como “alexina”, caracterizado frente al anticuerpo por su termolabilidad e inespecificidad (más tarde recibió el nombre de complemento, propuesto por Ehrlich), además de desarrollar -sin mucho éxito- la primera vacuna contra esta enfermedad. El apellido de esta señorita bacteria siguió siendo el original propuesto ya en 1679 por el médico inglés Thomas Sydenham, pertussis (por provocar mucha tos, claro).
Los dos investigadores eran francófonos pero Bordet, de origen belga, recibió el Nobel y la fama —era metódico, muy serio y genial— y Gengou, de origen francés, algo más prosaico y terrenal, quedó en un segundo plano, aunque en algunas publicaciones consideran belgas a los dos investigadores. Tan en segundo plano ha quedado para toda la historia el francés Gengou que no he podido encontrar en la red una sola imagen que nos pusiera cara y ojos a este colaborador inestimable de Bordet (le animo a conseguir una, amable lector, y no se confunda porque Wasserman y un ingeniero llamado también Octave, son los fallidos resultados que nos da Google cuando ponemos Gengou o Gengou Octave en la ventanita correspondiente).
Además de investigador, Bordet era “buena gente” y en 1924 se unió a un grupo de científicos que elaboraron un manifiesto contra el uso de gases tóxicos contra soldados en cualquier guerra (la primera guerra mundial estaba muy reciente) y en 1958 se adhirió a la manifestación de Linus Pauling de suspender ensayos con bombas nucleares. Pauling no era un cualquiera pues pocas personas pueden presumir de tener dos premios Nobel (de la paz y de Química).
Aunque nosotros la denominamos tosferina (tos de fiera, aunque no creo que muchos hayan oído toser a ningún tigre o león), en el mundo anglosajón se define como pertussis o whopping cough (whoop = chillido, grito; cough = tos; algo así como tos con sonido especial que parece un grito). Los franceses, sin embargo, son más originales y la llaman coqueluche. Hay varias teorías para explicar esta denominación: la más simple estriba en saber que “coq” en francés significa gallo, y el sonido que emite el enfermito al acabar la salva de tos se parece bastante a la fase final del canto de tan aguerrida y plumada ave. La teoría más elaborada supone conocer el nombre en francés de la capucha con que se cubría a los enfermos para evitar la expansión de bordetellas a tutiplén a su alrededor: coqueluchon, del latín cuccullio. Ya que estamos con el latín, la expresión a tutiplén viene de juntar «viciosamente» las palabras latinas: totus, todo y plenus, lleno.

Aunque ya sabían, pues, quien producía esa enfermedad que llevaba a la tumba a miles de niños en el mundo, no tenían tratamiento alguno para poder mitigar los terribles efectos de las toxinas que el germen liberaba en las mucosas de los inmaduros y delicados aparatos respiratorios de los bebés (hablaremos luego de estas toxinas), pues los agentes que inhibían el crecimiento de la bacteria en el laboratorio no podían ser tolerados por los enfermos. Como el ambiente rico en CO2 en el cultivo favorecía el crecimiento de la bacteria, a alguna mente privilegiada se le ocurrió pensar que un exceso de oxígeno sería letal para la elusiva Bordetella por lo que ni cortos ni perezosos comenzaron a poner niños afectados en los asientos delanteros de vehículos deportivos (aunque estemos en el 1917, no desprecien la potencia de un 6 cilindros con 7.500 cc, capaz de ponerse a 145 km/h en un santiamén) para someterlos a una aireación terapéutica:
Pero los experimentos no acabaron aquí, pues en 1927, un médico militar, “mejoró” el método para poder tratar a su regimiento de aviadores afectado por una epidemia de tosferina. Merece la pena transcribir sus propias palabras:
“Subir a una altura de 2.500 a 3.000 metros en diez a quince minutos, continuar máximo una hora a este nivel y luego hacer dos descensos pasajeros, en picada, de 500 metros cada uno; recuperar luego la altura, para descender finalmente al suelo a la misma velocidad de subida. El avión debe estar totalmente descubierto o al menos ampliamente comunicado al exterior”.
Es posible que estos audaces métodos fueran menos dañinos que los promulgados por otros facultativos que propugnaban inyecciones de éter, preparados de quinina, exposición a luz ultravioleta, vacunación con Bordetella viva, dar extracto de vesícula biliar de buey, hierbas chinas, inhalaciones de bencina o de ácido fénico o de cloroformo, morfina, tintura de opio, distintos bromuros; ofrecer cáñamo indio, belladona, cornezuelo de centeno e hidrato de cloral. Entremos en materia tras estos apuntes históricos:
TAXONOMÍA- ETIOPATOGENIA
La tosferina es una enfermedad contagiosa, muy contagiosa y no solo ataca a bebés y niños sino que también afecta a jóvenes y a personas adultas, ya que el padecimiento de la enfermedad no proporciona inmunidad para toda la vida, sino “solo” para unos 15 años aproximadamente (sin embargo el sarampión y la varicela suelen proporcionar casi siempre inmunidad «per vitam»). Salvo en menores de 4-6 meses, la enfermedad es molesta pero no suele ser grave y mucho menos mortal como ha sucedido en estos casos recientes.
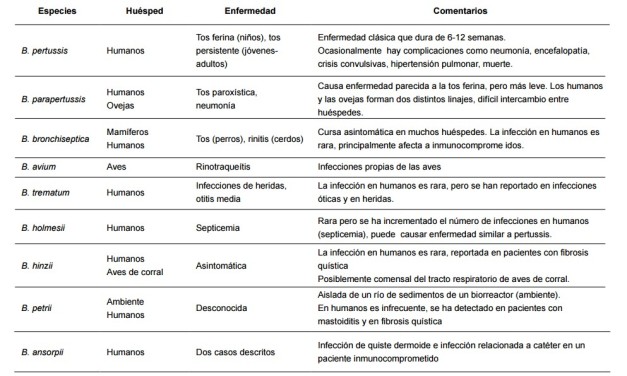
La Bordetella pertussis tiene “primas”, es decir, otras especies del género Bordetella (B), que también nos pueden afectar, como la B. parapertussis que causa una sintomatología más leve (se denomina cuadro seudopertusoide) y la B. bronchiseptica que produce infección respiratoria en diferentes especies animales, incluido el ser humano (donde aparentemente no produce tosferina) pero puede ser responsable de infección oportunista en pacientes inmunodeprimidos. Por último, B. avium también puede causar excepcionalmente enfermedad en humanos pero su diana son las aves como indica su apellido.
La diferenciación entre estas especies se realiza identificando diversas características bioquímicas y mediante técnicas inmunológicas. No hay inmunidad cruzada lo que quiere decir que podemos sufrir una infección por una especie y no desarrollar inmunidad con otras. Con denominaciones curiosas se recogen otras 4 especies de este género Bordetella: ansorpii (solo dos casos registrados en la casuística mundial), hinzii, holmesii (expresión emitida con honda emoción y elevado volumen por aficionados “culés” en muchos partidos) y trematum. Dejando el chistecito futbolero a un lado, en este enlace se describe un brote por esta especie de Bordetella en Chile. En este cuadro se puede ver un resumen de los diferentes huéspedes y patología de las especies conocidas de Bordetella:
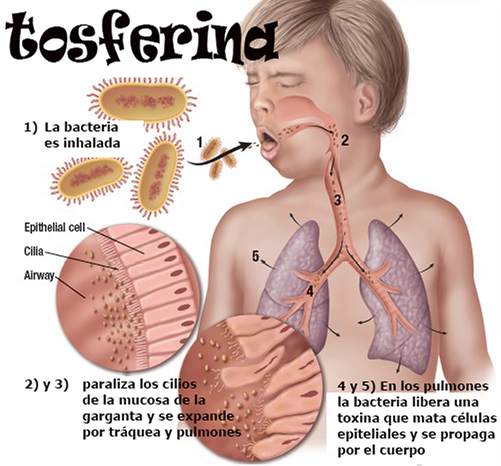
Esta bacteria sólo sobrevive unos minutos en el medio ambiente y por tanto, solo se transmite de persona a persona y no por utensilios y otros objetos. El mecanismo de transmisión es aéreo, a través de gotas de saliva contaminada que expulsa el enfermo al hablar, con la tos y los estornudos. Lógicamente, con besos «amorosos» y tiernos también se trasvasan Bordetellas o lo que haga falta.

Una vez que la Bordetella llega a la parte alta de nuestro aparato respiratorio se multiplica en la fina capa de moco que normalmente reviste nuestra mucosa y alcanza por contigüidad las estructuras vecinas. La capacidad de la bacteria de alcanzar las vías respiratorias y establecerse en ellas, adherida a las células ciliadas presentes en la superficie de nuestras
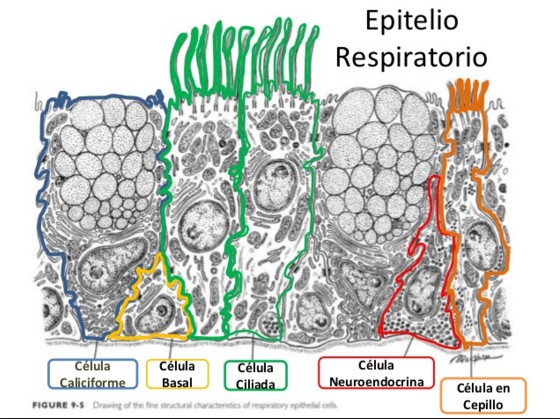
mucosas se debe a un conjunto de sustancias biológicamente activas, producidas por la bacteria, que desempeñan un papel en la inducción de la enfermedad. La primera de ellas es un monómero de peptidoglucano de la pared celular con afinidad por las células ciliadas, que constituye una toxina denominada citotoxina traqueal (TCT o traqueal cytotoxin), que inhibe la síntesis de ADN lo que impide la regeneración de las células dañadas y causa ciliostasia, es decir, hace que los cilios queden estáticos y no se muevan para arrastrar los productos que interesa despejar de las vías respiratorias: moco, restos de microorganismos muertos o fagocitados por nuestras defensas, partículas pequeñas de polvo u otros materiales que inhalamos diariamente, y eventualmente, la muerte de células epiteliales, produciendo lesiones locales en la mucosa que provocan el inicio de la tos. El factor de colonización traqueal (TCF) facilitaría la invasión de la tráquea; la hemolisina de Adenilato Ciclasa (Ac-Hly) y, posiblemente, la toxina pertusis (PT) ayudan a los organismos a protegerse de las células fagocíticas y pueden estimular la secreción de fluido y moco; también participan en este proceso la hemaglutinina filamentosa (FHA) que ayuda a las bacterias a pegarse a los cilios, el aglutinógeno fimbrial, la pertactina (PRN) y la BrkA (proteína de membrana externa que ofrece adherencia y resistencia al complemento). Una toxina dermonecrótica termolábil ayudaría a todo este conjunto de moléculas a provocar destrucción del tejido de nuestra mucosa respiratoria.
La bacteria no atraviesa las capas epiteliales, es la PT la encargada de entrar en la corriente sanguínea y provocar —alejada del árbol respiratorio— otros efectos como son: hipoglucemia, linfocitosis y sensibilización a la histamina, con aumento de inmunoglobulina E (IgE) y de interleucina 4 (IL4) . Después, la PT empieza a producir efectos locales y/o sistémicos exacerbando la tos, que se ha producido en respuesta a la irritación y el daño local. La PT, la Ac-Hly y el BrkA tienen marcados efectos sobre el sistema inmunológico del huésped. El último factor de tan tenebrosa pandilla sería un lipopolisacárido (LPS) con las mismas actividades que el de otras bacterias Gram negativas: pirogenicidad (capacidad de producir fiebre), toxicidad e inducción inespecífica de interferón; el LPS está compuesto por dos lípidos llamados «A» y «X» y dos cadenas de oligosacáridos. El lípido X posee la actividad clásica de las endotoxinas y el lípido A tiene menor pirogenicidad pero es un potente coadyuvante y estimula la secreción de interleucina 1.
Las lesiones del epitelio respiratorio producen exudados con moco, sangre y pus que comprometen la permeabilidad de las vías respiratorias de menor tamaño, especialmente en los más pequeños, lo que predispone a la aparición de neumonías y atelectasias (zonas del pulmón retraídas o colapsadas).
Todas estas secuencias pueden explicar las manifestaciones respiratorias de la tosferina, pero en algunos casos también hay manifestaciones fuera del aparato respiratorio, cuya patogenia no queda muy clara. En este dibujo podemos observar casi todas las toxinas y adhesinas involucradas en la patogenicidad (capacidad de generar enfermedad) de semejante bichejo:

La expresión de la mayoría de factores de virulencia, necesarios para la colonización de personas susceptibles está regulada por el sistema de “Genes de Virulencia de la Bordetella” (BvgAS), conociéndose tres tipos; BvgA, BvgS y BvgR respectivamente. Este sistema genético media en su activación de Bvg+ y Bvg- como consecuencia de cambios y estímulos a nivel del ambiente, tales como cambios de temperatura, concentración de ácido nicotínico y sulfatos.
¿No pensáis que después de toda esta entretenida descripción de toxinas presentes en la superficie de esta terrible bacteria, podríamos representarla de esta manera más fácil de recordar? (esquema realizado a partir de una imagen de esta web) :

Veamos ahora dos imágenes de dos de estas toxinas, ahora ya sin fantasía:
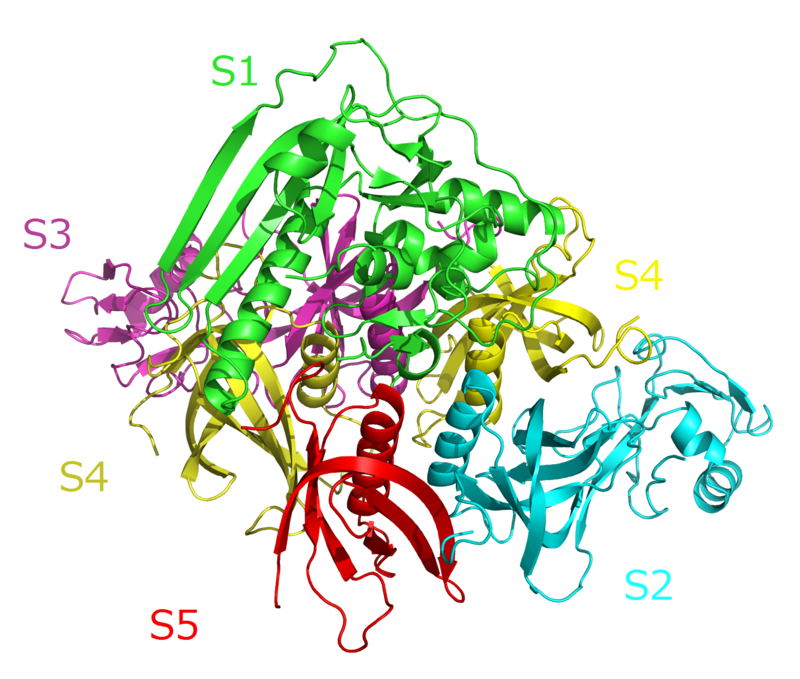
1) Estructura molecular de la Toxina pertúsica con sus 5 subunidades:
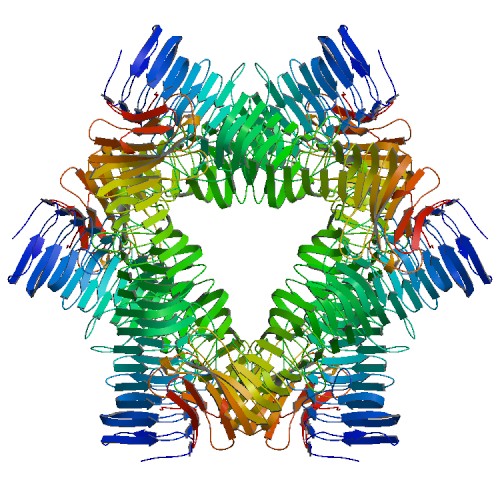
2) Pertactina



Increible descripción!!!
Me gustaMe gusta
Gracias sinceras.
Perdón por el retraso.
Me gustaMe gusta
Muy interesante y completo!! Gracias por el post
Anna
Me gustaMe gusta
Lo dicho.
Me gustaMe gusta
Post muy útil sobre una enfermedad que afecta a los más pequeños e indefensos i sobretodo ¡prevenible! Y muy buena descripción a nivel histórico, bioquímico y epidemiológico de la tos ferina
Me gustaMe gusta
No podemos hacer más que darte las gracias por tu aportación y por los halagos.
Me gustaMe gusta
Gracias por tu aportación y aprobación, Anna.
Me gustaMe gusta